Das Glioblastom ist der tödlichste aller Hirntumore, nun ist ein internationales Forscherteam auf eine chemische Verbindung gestoßen, die zur Entwicklung einer ganz neuen Wirkstoffklasse führen könnte. In der im Fachmagazin Science Transnational Medicine publizierten Studie, zerstörten sich Glioblastomzellen nach Kontakt mit der Substanz selbst. Ein Hoffnungsschimmer im Kampf gegen den tödlichsten aller Hirntumore.
Bis zu 24.000 Hirntumore pro Jahr
In Europa erkranken jedes Jahr etwa zwei bis drei von 100.000 Einwohnern, also rund 16.000 – 24.000 Menschen, an einem tödlichen Hirntumor. Das mittlere Erkrankungsalter liegt bei 64 Jahren, wobei Männer im Durchschnitt etwas häufiger erkranken als Frauen. Das Glioblastom, ein bösartiger Tumor der Gliazellen, zählt zu den aggressivsten aller bekannten Hirntumore. Obwohl in den letzten 30 Jahren viel geforscht wurde, ist der Tumor bisher nicht wirksam behandelbar.
So haben beispielsweise alle neu entwickelten Medikamente der jüngsten Zeit das Überleben der Betroffenen gerade einmal um drei Monate verlängert. Die Diagnose Glioblastom ist deshalb noch immer ein Todesurteil, die 5-jährige Überlebensrate liegt aktuellen Krebsstatistiken zufolge gerade einmal bei drei Prozent.
Selbst wer die zehrende Therapie, die aus Operation, Bestrahlung und nicht besonders wirksamer Chemotherapie besteht, über sich ergehen lässt, lebt in vielen Fällen nicht viel länger als zwei Jahre. Die Mehrzahl der Erkrankten stirbt sogar innerhalb eines Jahres nach der Diagnose.
Größte Hürde, die Blut-Hirnschranke
Dass Hirntumore besonders schwer zu behandeln sind, liegt an einer ganz besonderen Herausforderung — der Blut-Hirnschranke. Diese selektive Barriere, deren Epithelzellen über sogenannte Tight Junctions eng miteinander verknüpft sind, wirkt wie ein Filter und lässt nur ganz ausgewählte Moleküle passieren. Was eigentlich dem Schutz des Gehirns dient, entwickelt sich im Kampf gegen den Krebs als eine der größten Hürden, denn den allermeisten Stoffen bleibt der Weg ins Gehirn verwehrt.
Vor diesem Hintergrund ist das Gemeinschaftsprojekt der University of Leeds, dem Leeds Teaching Hospital Trust, dem Cancer Research UK Cambridge Institute, der University of Huddersfield, dem California Institute for Biomedical Research und der University of California ein echter Hoffnungsschimmer im Kampf gegen diesen aggressiven Tumor.
Zuversichtliche Wissenschaftler
Auch wenn der potenzielle Hoffnungsträger zum gegenwärtigen Zeitpunkt nicht viel mehr als Grundlagenforschung ist, und bis zu einem ersten hoffnungsvollen Medikament wohl noch Jahre vergehen dürften, sind die beteiligten Wissenschaftler zuversichtlich. Dabei ist ihre neue Waffe gegen den Krebs weder eine innovative Gentherapie noch ein spektakulärer neuer Antikörper, sondern ein ziemlich einfaches synthetisches Molekül, dass vor allem durch seinen sperrigen chemischen Namen — N4-isobutyl-N2-((2-phenylthiazol-4-yl)methyl)pyrimidine-2,4-diamine — Aufmerksamkeit auf sich zieht.
Bekannter ist die Verbindung unter der Kurzbezeichnung KHS101. Die chemische Substanz bindet an eine Proteinstruktur des Centrosoms und des mitotischen Spindelapparates im Zellkern und löst so die Differenzierung neuronaler Vorläuferzellen aus. Schon Polson et al. wiesen darauf hin, dass Stammzellen — also undifferenzierte Zellen — zum aggressiven Wachstum des Glioblastoms beitragen können, und dass Stoffe wie KHS101, die eine Differenzierung von Zellen einleiten, vermutlich auch eine therapeutische Wirkung besitzen könnten.

Heiko Wurdak mit Kollegen in seinem Labor an der Universität Leeds. Quelle & Rechte: Stem Cells and Brain Tumour Group, University of Leeds
Diese Idee griff nun ein Forscherteam unter Leitung von Heiko Wurdak von der britischen Universität Leeds auf und testete mögliche Wirkungen der Substanz im Labor- und Tierversuch.
Gesunde Zellen bleiben verschont
Die Ergebnisse waren mehr als überraschend, meint Wurdak, denn die Glioblastom-Zelllinie, die mit KHS101 in Kontakt kam, zeigte nicht nur die erwartete Wachstumshemmung, vielmehr zerstörten sich die Krebszellen gleich selbst. Doch was bei Zellen funktioniert, muss noch lange nicht im Gehirn funktionieren. Denn um eine tödliche Wirkung im Gehirn zu entfalten, muss KHS101 zuerst einmal die Blut-Hirnschranke passieren.
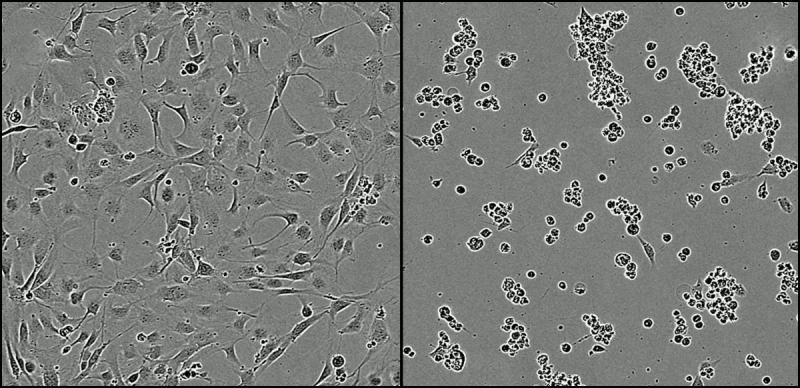
Normale Tumorzellen (links) und mit KHS101 behandelte abgestorbene Tumorzellen (rechts). Quelle & Rechte: Stem Cells and Brain Tumour Group, University of Leeds
Ob ihm dies gelingt testeten die Forscher in einem Mausmodell. Dazu transferierten sie Glioblastomzellen von Menschen in Mäuse, verabreichten diesen KHS101 und untersuchten anschließend den Verlauf des Tumorwachstums. Zu ihrer Überraschung gelangte die Substanz wohl problemlos über die Blut-Hirnschranke, denn das Tumorwachstum der behandelten Tiere verringerte sich um 50 Prozent. Zudem lebten die mit KHS101 behandelten Tiere deutlich länger als die unbehandelten Kontrolltiere.
Besonders vielversprechend sei auch die Tatsache, dass gesunde Zellen scheinbar nicht beeinträchtigt würden, meint Studienleiter Wurdak. Denn dies würde schließlich bedeuten, dass eine mögliche Therapie keinerlei Nebenwirkungen hätte. Und noch ein weiterer Pluspunkt spricht für KHS101: Sämtliche Zellen des Tumors, die sich in ihrer Genetik oftmals drastisch unterscheiden, sprachen auf die experimentelle Behandlung an.
KHS101 könnte also, sollte es den langen Weg bis zu einer Zulassung überstehen, tatsächlich eine vielversprechende neue Waffe im Kampf gegen das aggressive Glioblastom werden.
Keine Energie für Krebszellen
Wie KHS101 es anstellt, dass Tumorzellen innerhalb kurzer Zeit sterben, ist im Ansatz bekannt: Das Molekül soll in den Mitochondrien das Hitzeschockprotein D1 (HSPD1) in seiner Funktion derart einschränken, dass der gesamte Energiestoffwechsel der Zelle lahm gelegt wird. Auf diese Weise schneidet es Tumorzellen von ihrer Energieversorgung ab, was zu deren Tod führt.
Auch wenn diese ersten Ergebnisse vielversprechend sind, Studien am Menschen werden noch auf sich warten lassen, und bis zu einer möglichen Therapie könnte es sogar noch Jahre dauern. Dass die neu entdeckten HSPD1-abhängigen Stoffwechselwege zu einer effektiven Strategie im Kampf gegen das Glioblastom und andere bösartige Hirntumore werden, davon sind die Forscher allerdings überzeugt.
Deshalb haben sie auch schon die nächsten Schritte geplant: Zuerst wollen sie die Eigenschaften im Detail studieren, die KHS101 zu einem effizienten Krebskiller machen, und sich anschließend auf die Suche nach ähnlichen Substanzen machen, um so die Chancen auf ein Medikament zu erhöhen.
Dass die Ergebnisse nur ein erster Schritt in einem noch langen Prozess sind, ist Wurdak bewusst, sie würden aber der Wirkstoffforschung erstmalig einen hoffnungsvollen neuen Weg zu wirksameren Medikamenten gegen bösartige Hirntumore aufzeigen, meint der Forscher.